Brasil assina memorando com Pfizer, afirma Ministério
A farmacêutica ainda não pediu autorização junto à Anvisa
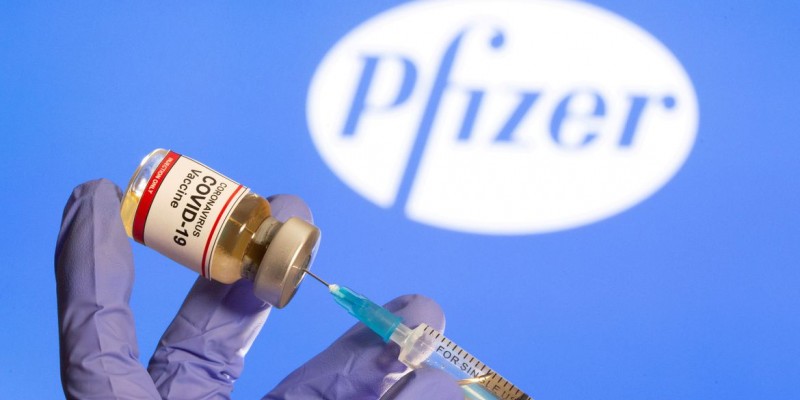
Foto: REUTERS/Dado Ruvic - via ABR
Por Agência Brasil
O governo federal assinou um memorando de entendimento com a Pfizer, empresa que desenvolve uma das vacinas contra a covid-19. Contudo, a farmacêutica ainda não deu entrada em pedido de registro ou de autorização emergencial junto à Agência Nacional de Vigilância Sanitária (Anvisa).

A informação foi dada ontem (10), em entrevista coletiva de secretários do Ministério da Saúde, em Brasília.
Segundo o secretário executivo da pasta, Élcio Franco, o memorando prevê inicialmente 8,5 milhões de doses no primeiro semestre de 2021 e 61,5 milhões no segundo semestre. São necessárias duas doses para imunizar um paciente contra a covid-19. Ele acrescentou que o memorando ainda não detalha as quantidades de doses por mês.
Perguntado sobre a afirmação do ministro Eduardo Pazuello sobre a possibilidade do início da vacinação em dezembro, o secretário respondeu que esta alternativa depende de uma conjunção de fatores.
“Quando se fala em dezembro, em conseguindo a autorização em usos emergencial e conseguindo também [a Pfizer] nos disponibilizar, teríamos condição de iniciar em dezembro. Mas depende da autorização para uso emergencial da Anvisa e disponibilização das doses”, comentou.
Ele acrescentou que não será toda a população. Grupos que não participaram da Fase 3, como gestantes e crianças, não têm garantia de segurança e eficácia e, portanto, ficarão de fora a menos que uma vacina esteja disponível com estudos que comprovem a ação nesses segmentos.
Franco lembrou que nem a Pfizer nem qualquer outra farmacêutica entrou ainda com pedido de registro ou autorização emergencial na Anvisa. A primeira envolve a liberação da licença normal da agência.
Já a segunda consiste em uma permissão especial com requisitos específicos definidos pela Anvisa. Ela só poderá ser solicitada por empresas com testes clínicos no Brasil, em caráter temporário e para públicos específicos.
A legislação também prevê a alternativa de uma análise rápida pela Anvisa caso uma vacina tenha obtido o registro em agências reguladoras de medicamentos nos Estados Unidos, União Europeia, Japão ou China. Nenhuma das vacinas em estudo pelo governo brasileiro obteve ainda registro nestes países.
Além do memorando com a Pfizer, foi firmado um acordo de encomenda tecnológica com o consórcio da Universidade de Oxford e da Astrazeneca, que em parceria com a Fundação Oswaldo Cruz.
Ontem a presidente da instituição, Nísia Trindade, informou em um seminário que a perspectiva é de 30 milhões de doses até fevereiro, 70,4 milhões entre março e agosto e mais 100 milhões após este período, totalizando 210 milhões de doses.
Notícias Relacionadas
- Por REDAÇÃO
- 28/08/2023
Centro de testagem para Covid-19 da Prefeitura do Recife está em novo local
Novo local também é na Iputinga
- Por REDAÇÃO
- 11/05/2023
Câmara aprova criação do dia em memória de vítimas de COVID-19
Até a última atualização apresentada pelo Conselho Nacional dos...
- Por REDAÇÃO
- 02/05/2023
COVID-19: Brasil tem o primeiro caso da variante Arcturus
A variante arcturus pode causar, além dos sintomas tradicionais, uma...
- Por REDAÇÃO
- 26/04/2023
Recife inicia vacinação bivalente contra COVID-19; mais de 500 mil habitantes podem tomar o imunizante
As vacinas bivalentes contra a COVID-19 protegem contra a cepa original do...
- Por REDAÇÃO
- 25/04/2023
Pela baixa adesão, governo amplia vacina bivalente para todos acima de 18 anos
As vacinas bivalentes contra a COVID-19 protegem contra a cepa original do...
- Por REDAÇÃO
- 21/04/2023
COVID-19: Vacinação bivalente não precisa de agendamento no Recife
Segundo a Gestão Municipal, “para o atendimento, é necessário...