A Anvisa tem 30 dias para avaliar o pedido.
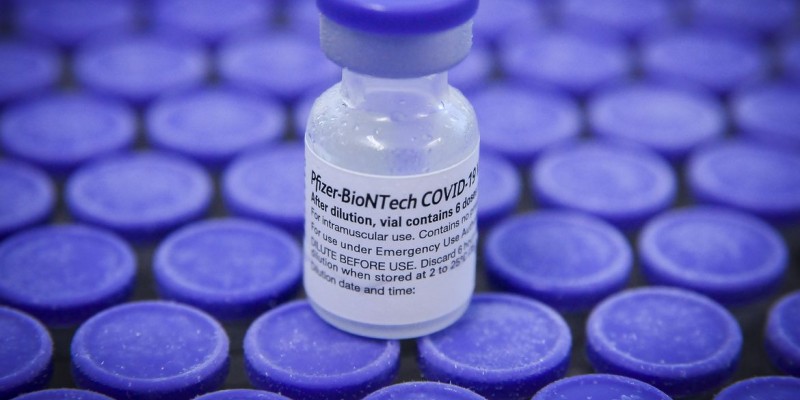
Foto: Geovana Albuquerque / Agência Saúde DF
A empresa farmacêutica Pfizer enviou à Agência Nacional de Vigilância Sanitária (Anvisa) um pedido de autorização de uso emergencial de uma segunda vacina contra a Covid-19. Essa nova vacina é bivalente, o que significa que agr no organismo contra duas cepas do vírus. É uma mistura da cepa original aplicada desde fevereiro de 2021, com a cepa da Ômicron.
A Anvisa tem 30 dias para avaliar o pedido. Esse prazo deve ser interrompido à medida que seja necessária a solicitação de complementos de informação ou esclarecimentos.
O primeiro país a aprovar uma vacina para combater a Ômicron foi o Reino Unido, onde o órgão regulador equivalente à Anvisa aprovou após ensaios clínicos que apontaram “forte resposta imune” contra a Ômicron.
Ouça a notícia com o repórter João Paulo Ribeiro, clicando no 'play' acima.
Notícias Relacionadas
- Por REDAÇÃO
- 17/05/2024
Dia Mundial da Doação de Leite Humano reforça a importância da ação
A SES realiza todo o processo, desde a coleta até a distribuição do leite...
- Por REDAÇÃO
- 17/05/2024
Cuida PE realiza mutirão com mais de 3 mil exames em unidades de saúde do estado
Atendimentos serão nas UPAEs distribuídas em vários municípios de...
- Por REDAÇÃO
- 17/05/2024
Arboviroses: Pernambuco começa a testagem para Febre do Oropouche
A doença é um vírus transmitido pelo mosquito Culex quinquefasciatus,...
- Por REDAÇÃO
- 16/05/2024
Pernambuco tem 103 bebês e crianças à espera de leito em UTIs neonatal e infantil, diz SES
O número é registrado após a fila por vaga em UTI ter batido recorde nesta...
- Por REDAÇÃO
- 15/05/2024
Pernambuco identifica número de queda da incidência de dengue no Estado
No último boletim epidemiológico, o indicador apontava 278,7 casos...
- Por REDAÇÃO
- 15/05/2024
Pernambuco confirma quarta morte por dengue; homem de 79 anos morava em Moreno
Segundo a SES, o idoso possuia outras comorbidades e veio à óbito no dia 05...






