A Anvisa tem 30 dias para avaliar o pedido.
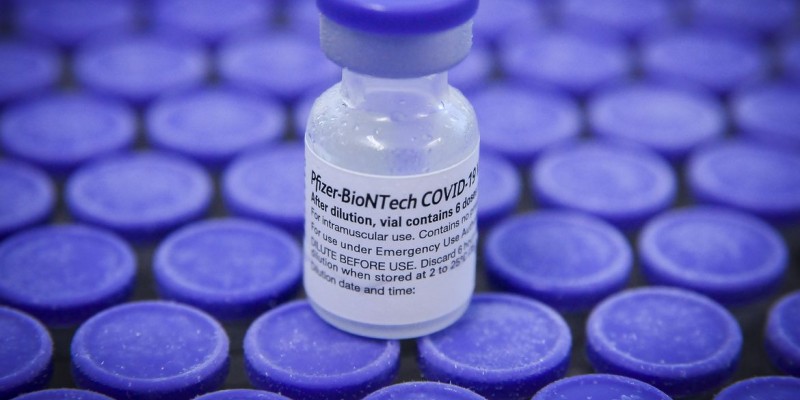
Foto: Geovana Albuquerque / Agência Saúde DF
A empresa farmacêutica Pfizer enviou à Agência Nacional de Vigilância Sanitária (Anvisa) um pedido de autorização de uso emergencial de uma segunda vacina contra a Covid-19. Essa nova vacina é bivalente, o que significa que agr no organismo contra duas cepas do vírus. É uma mistura da cepa original aplicada desde fevereiro de 2021, com a cepa da Ômicron.
A Anvisa tem 30 dias para avaliar o pedido. Esse prazo deve ser interrompido à medida que seja necessária a solicitação de complementos de informação ou esclarecimentos.
O primeiro país a aprovar uma vacina para combater a Ômicron foi o Reino Unido, onde o órgão regulador equivalente à Anvisa aprovou após ensaios clínicos que apontaram “forte resposta imune” contra a Ômicron.
Ouça a notícia com o repórter João Paulo Ribeiro, clicando no 'play' acima.
Not��cias Relacionadas
- Por REDAÇÃO
- 01/08/2025
Criança é diagnosticada com meningite tipo B em Garanhuns, mas apresenta melhora
Caso raro da forma bacteriana grave da doença foi confirmado por exame;...
- Por REDAÇÃO
- 01/08/2025
Projeto da UFPE busca voluntárias para pesquisa sobre câncer de mama
As mulheres irão receber uma avaliação física e cardiológica e acesso ao...
- Por REDAÇÃO
- 31/07/2025
Prefeitura disponibiliza duas mil vagas em Mamógrafo Móvel em bairros do Recife; confira
Ao todo, veículo irá circular por 25 locais diferentes em agosto
- Por REDAÇÃO
- 31/07/2025
Secretaria de Saúde de Pernambuco confirma quinta morte por dengue em 2025
A vítima foi um homem de 74 anos, morador de Ouricuri, no Sertão
- Por REDAÇÃO
- 29/07/2025
Estado anuncia vacina contra hepatite A para quem utiliza Profilaxia Pré-Exposição ao HIV; entenda
Disponibilização do imunizante acontece após recente alta em casos no...
- Por REDAÇÃO
- 24/07/2025
Recife realiza Dia D de combate às Hepatites Virais com ações em oito pontos da cidade
Mobilização acontece neste sábado (26) com testagens, vacinação,...








